


前言
以嵌合抗原受体(CARs)为基础的T细胞治疗已显示出对血癌的巨大成功;然而,潜在的致命毒性(如细胞因子释放综合征)和高成本是限制CAR-T细胞临床应用的一些缺点,有待克服。
自然杀伤(NK)细胞是当前免疫学研究的焦点,迄今为止,利用NK细胞治疗恶性肿瘤已经取得了一定的成功。NK细胞受体生物学的最新进展极大地改变了我们对NK细胞如何识别和杀死肿瘤细胞的理解。CAR-NK细胞由于其独特的识别机制、强大的细胞毒性作用以及临床安全性,成为癌症再靶向治疗的强力候选。此外,NK细胞降低了同种异体反应的风险,可以作为“现成产品”。
虽然目前如火如荼的CAR-NK疗法依然面临着许多挑战和障碍,但其巨大的潜力已经在肿瘤免疫治疗领域展现出广阔的前景。
NK细胞是第一个被鉴定的先天性淋巴细胞(ILC)亚型,能对病毒感染和/或转化的细胞产生多种效应器功能,主要是细胞杀伤和产生促炎细胞因子。NK细胞和其他ILC家族成员(ILC1s、ILC2s和ILC3s)与B细胞和T细胞来源于相同的淋巴祖细胞。NK细胞的细胞毒性活性使它们在功能上与CD8+T细胞最为相似,而ILC1、ILC2和ILC3群体的细胞因子生成模式将这些细胞分别对应CD4+T细胞的TH1、TH2和TH17亚群。
NK细胞的两个最典型的亚群是CD56brightCD16-和CD56dimCD16+群体。CD56bright细胞在外周血中的数量较少(循环中90%的NK细胞是CD56dim),而组织中的NK细胞主要是CD56bright。CD56bright NK细胞是强有力的细胞因子产生者,除非受到促炎性细胞因子如IL-15的刺激,否则细胞毒性较弱。相比之下,CD56dim NK细胞群可介导感染细胞和恶性细胞的连续杀伤,主要通过包含颗粒酶B和穿孔素的预先组装的溶细胞颗粒在免疫突触中的胞吐,最终诱导靶细胞凋亡。
与B细胞和T细胞不同,NK细胞不表达体细胞重排的抗原受体,而是激活受体和抑制受体的随机组合。通过这些不同受体的刺激信号与抑制信号的平衡产生对靶细胞的反应或耐受。MHC-I(主要组织相容性复合物Ⅰ类)抗原特异性的抑制性受体可密切调节NK细胞介导的细胞毒性和淋巴因子的产生。MHC-I特异性受体的抑制信号对于造血细胞避免NK细胞的破坏至关重要。这个概念被称为“丢失自我”,最初是由 Ljunggren和Karre 提出的。这种MHC-I识别抑制性受体形成了NK细胞表面受体的三个家族,即KIRs(杀伤细胞免疫球蛋白样受体)、LIRs(白细胞免疫球蛋白样受体)和NKG2A(自然杀伤细胞2族A)。
KIRs是免疫球蛋白超家族的成员,是识别经典人类白细胞抗原A、B和C(HLA-Ia类)的I型跨膜分子。LIRs又称ILTs(免疫球蛋白样转录物),形成第二组受体,除了HLA Ia类外,主要识别非经典HLA-G(Ib类)分子。LIRs与KIRs属于同一个Ig超家族。NKG2A是NKG2族的一个成员,包括A、B、C、D、E、F和H,与CD94二聚形成NKG2A/CD94受体。它属于受体的C型凝集素家族,识别非经典HLA-EⅠ类分子作为其配体。
NK细胞的杀伤作用不仅需要通过抑制性受体检测转化细胞上的MHC-I分子,还需要通过激活性受体激活NK细胞。自然细胞毒性受体(NCR)是一组自然杀伤细胞表面激活性受体,包括NKp46、NKp30和NKp44。这些受体以及NKG2D和DNAM-1(DNAX辅助分子-1)识别病毒感染或恶性转化细胞表面表达的配体。一些共受体(2B4、NKp80、NTB-A和CD59)也被表达,它们只有与其他激活性受体结合才能发挥作用。CD16(或FcγRIII)也是一种激活性受体,主要由CD56dim NK细胞亚群表达,对IgG包被靶细胞的抗体依赖性细胞毒性(ADCC)至关重要。
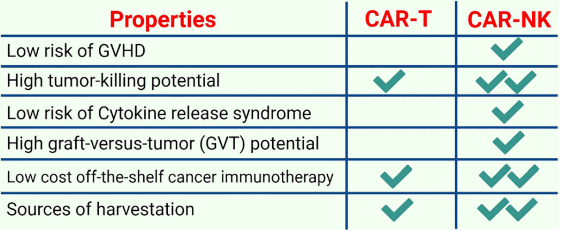
CAR-NK细胞和CAR-T细胞一样存在胞外、跨膜和胞内信号传导域。NK细胞通过另外两个共刺激分子,即NKG2D和CD244(2B4)增加其细胞毒性能力和细胞因子的产生。因此,比CAR-T细胞具有更强的肿瘤特异性靶向性和细胞毒性。CAR-NK细胞疗法可能在未来成为CAR-T疗法的替代方案,因为CAR-NK细胞具有以下超越CAR-T的几个独特特征。
首先,异基因NK细胞对于过继性细胞治疗(ACT)是相当安全的,因为它们通常不介导发生GVHD。此外,NK细胞仅分泌少量IFN-γ和GM-CSF,不产生启动CRS的IL-1和IL-6。其次,除了通过单链抗体识别肿瘤表面抗原来抑制癌细胞外,NK细胞还可以通过多种受体识别各种配体来抑制癌细胞,例如自然细胞毒性受体(NKp46、NKp44和NKp30)、NKG2D和DNAM-1(CD226)。最后,NK细胞在临床样本中非常丰富,可以从外周血(PB)、脐带血(UCB)、人类胚胎干细胞(HESC)、诱导多能干细胞(IPSC)甚至NK-92细胞系中产生。
CAR-NK疗法的研究目前处于起步阶段,临床研究的数量逐年增加。此外,在研究的靶标方面,CD19抗原在血液肿瘤中最常见。在实体瘤中进展最为广泛的CAR-NK疗法包括肿瘤相关抗原HER2、MUC1和PMSA等靶点。
目前,一些正在进行的临床试验正在调查CAR-NK细胞治疗血液学肿瘤和实体瘤的安全性和有效性,这些试验在下表列出。
低持久性
在缺乏细胞因子支持的情况下,输注细胞缺乏体内持久性是过继NK细胞治疗的主要缺点之一。虽然它可能更安全的,但它也会限制NK细胞免疫治疗的效果。外源性细胞因子已被证明能增加过继性NK细胞的增殖和耐久性;然而,它们也可能导致不希望的副作用,包括抑制性免疫亚群的生长,如Tregs。
转移到所需的肿瘤部位
快速归巢到肿瘤床对于过继性细胞治疗效果至关重要,并且受NK细胞和肿瘤细胞释放的趋化因子之间复杂相互作用的控制。然而,NK细胞归巢到肿瘤部位的效率一直存在争议,因此促使人们不断努力去进行改进。
一些研究人员已经研究了各种工程方法来改善NK细胞归巢。例如,用编码趋化因子受体CCR7的mRNA电穿孔NK细胞,以增加向表达趋化因子CCL19的淋巴结的移动。用编码CXCR2的病毒载体转导的NK细胞对表达同源配体如CXCL1、CXCL2、CXCL5、CXCL6和CXCL8的肾细胞癌肿瘤表现出更好的运动性。为了提高实体瘤患者NK细胞免疫治疗的成功率,在小鼠模型中研究了几种促进NK细胞向肿瘤部位转运的新技术;然而,这些方法的有效性还需要在临床试验中进行验证。
免疫抑制肿瘤微环境
TME包括免疫抑制分子、免疫抑制细胞和妨碍免疫细胞功能的不利环境,是CAR-NK细胞治疗的主要障碍。TGF-β;腺苷;吲哚胺2,3-双加氧酶(IDO)和前列腺素E2(PGE2)是TME中发现的可损害NK细胞活性的免疫抑制细胞因子和代谢物。Treg细胞;调节性B细胞;髓源性抑制细胞;肿瘤相关巨噬细胞(TAM);血小板;成纤维细胞和一些不利的代谢因素,如缺氧、酸度和营养缺乏,在恶性环境中会导致免疫抑制。
因此,研究人员正致力于开发能够防止某些免疫抑制作用的CAR-NK细胞。例如,通过使用CRISPR/Cas9技术敲除TGF-βR2基因或者阻断NK细胞上的高亲和力A2A腺苷受体。TME导致NK细胞耗竭的另一个重要方法是免疫检查点分子。为了克服这个问题,基因组编辑被用来消除NK细胞的检查点成分,以改善其功能。
慢病毒低转导效率
基于慢病毒的转导系统是细胞内基因修饰和传递的最常用的方法之一。然而,由于自然特性,NK细胞对慢病毒具有抗性,这使得基于慢病毒的转导成为一个挑战。为了改进病毒转导,人们使用了各种化学物质,例如,可以使用鱼精蛋白硫酸盐或葡聚糖去除细胞膜上的电荷。
识别靶抗原
CARs设计中最关键的一步是识别高度一致表达的靶肿瘤抗原。大多数肿瘤相关抗原(TAAs)也由一些健康细胞表达,因此,不可避免带来“靶向非肿瘤”的效应。此外,同一肿瘤的单细胞克隆中这些TAA的表达可能存在巨大差异。为了克服这个问题,人们设计了双特异性CAR,可以同时靶向多个抗原。
这可以通过多种方式实现,例如,可以同时注射针对不同抗原的不同CAR-NK细胞;或者设计一种能够识别多种抗原的CAR,这一目标可以通过“串联CAR”实现,其中两个结合点连接到单个分子上,以提高免疫突触的效率。此外,通过使用一个称为“双顺反子CAR”的载体可以在同一免疫细胞上产生多个CAR。
提高NK细胞活性
几个免疫检查点调节和抑制NK细胞活性。这些免疫检查点起到了“天然刹车”的作用,以防止自身免疫疾病或过度激活引起的免疫病理状况。这些检查点的基因缺失或阻断可以帮助CAR-NK细胞保持过度活跃,更快地摆脱癌症和转移。
例如,一种新的NK-92细胞系被设计成靶向PD-L1、ER保留的IL-2和高亲和力CD16的CAR,称为PD-L1靶向haNK(t-haNK)。令人兴奋的临床前数据表明,这些细胞在体外对15种肿瘤细胞株具有特异的抗肿瘤作用,在体内对三阴性乳腺癌、膀胱肿瘤和肺癌具有很强的抗肿瘤作用。
另一个提高CAR-NK细胞活性的重要策略是肿瘤代谢的调节,但这一策略尚未得到应有的重视。在缺氧条件下,腺苷是通过CD39和CD73代谢ATP产生的,它们参与免疫逃避,阻止NK细胞运输到肿瘤部位,并阻止NK细胞成熟。NKG2D工程化的CAR-NK细胞在抗CD73抗体抑制后显示出治疗肺癌的良好效果。
克服免疫抑制微环境
肿瘤具有多种免疫抑制因子,如TGF-β、IL-10、PD-1或精氨酸酶。有几种方法可以降低TGF-β的抑制作用。例如,TGF-β激酶抑制剂和NK细胞的组合被发现可以恢复NK细胞的细胞毒性,并且保留NKG2D和CD16的表达。此外,使用带有细胞外TGF-β受体结构域的混合型CARs已被发现在提高NK-92细胞的抗肿瘤潜能方面相当成功。通过敲除实体瘤中的SMAD3,NK细胞的细胞毒性活性已得到增强。
提高安全性
提高基于CAR-NK细胞治疗安全性的重要方法可能包括通过加入自杀基因或开发双特异性CAR分子来修饰CAR结构,以更好地靶向肿瘤特异性抗原。
CAR-NK细胞可以以CAR依赖和CAR非依赖的方式同样靶向肿瘤;因此,NK细胞的这一特性可以被用来发挥增强的肿瘤杀伤作用和开发非信号CAR。这些非信号CAR缺乏直接杀伤信号,但通过促进NK细胞在靶细胞上的驻留和粘附,可以增强NK细胞的特异性杀伤。另一个有趣的策略是设计能够调节TME的CAR-NK,这种CAR-NK被命名为“装甲”CAR-NK细胞。这些非常特殊的CAR-NK细胞表达几种外源基因,可以调节局部TME以防止任何有害影响。
提高可及性
为了克服实体瘤中CAR-NK细胞的可及性,可以使用几种方法,包括局部给药、腹腔给药和聚焦超声引导给药。例如,在模拟人类胸膜恶性肿瘤的原位模型中发现胸膜注射非常有效,其功能持续时间甚至比静脉注射获得的时间更长。局部给予CAR免疫细胞也可能有助于减少治疗剂量。
总的来说,NK细胞免疫生物学领域的进展和进步为更好和更新颖的免疫疗法奠定了基础,NK细胞优秀的抗肿瘤作用使其成为细胞免疫治疗的焦点。CAR-NK细胞疗法是一个很有前途的临床研究领域,与CAR-T细胞相比,CAR-NK细胞具有自己独特的优点,但仍面临着一些挑战。这些挑战包括细胞的持久性,克服免疫抑制微环境,以及转导效率等。相信解决好这些问题,基于NK细胞优秀的抗肿瘤血统,极有可能在CAR修饰的武装下为肿瘤治疗带来新的突破。
